디앤디파마텍은 18일 GLP-1/GCG 이중작용제 후보물질 ‘DD01’의 대사이상 관련 지방간염(MASH) 임상2상에서 주요 임상지표의 24주차 2차종결점에서 유의미한 개선효과를 확인했다고 밝혔다.
DD01은 디앤디파마텍이 자체 개발한 GLP-1 및 글루카곤 수용체를 동시에 타겟하는 장기 지속형 이중작용제 후보물질이다. 현재 미국에서 MASLD/MASH 환자를 대상으로 48주 투약 임상2상이 진행중이다.
현재 모든 환자가 DD01을 투약 종료 또는 30주 이상 투약을 진행 중이다. 이에 따라 간 조직생검 결과를 포함한 최종 주요 2차 평가지표 결과는 2026년 상반기 중 발표될 것으로 예상된다.
디앤디파마텍은 지난 6월 MRI-PDFF로 측정한 12주차 결과에서 지방간이 30% 이상 감소한 환자 비율과 평균 지방간 감소율 모두에서 위약 대비 통계적으로 유의미한 결과를 확인하며 1차종결점을 충족시켰다. 이는 글로벌 경쟁기업의 24~72주 장기투여 대비 경쟁력 있는 결과라는게 회사측의 설명이다.
디앤디파마텍은 이번 24주차 분석에서 2차종결점인 섬유화 관련 혈액 바이오마커를 분석했다. 또한 MASH 환자에서 높은 비중으로 동반되는 비만, 당뇨와 관련된 체중 및 혈당 결과를 함께 평가했다.
또, 48주 투여 후 확인 예정인 조직생검과 연계해 임상적으로 주요한 환자군인 F2-F3 단계 섬유화를 동반한 MASH 환자에 대한 하위그룹 분석도 추가로 수행했다.
그 결과 12주차에서 의미 있는 개선을 보였던 섬유화 관련 바이오마커(ELF Score, PRO-C3)는 24주차에도 위약군 대비 지속적인 개선을 보여 DD01의 효과가 지속됨을 확인했다.
섬유화 진행여부를 비침습적으로 평가하는 ELF Score는 위약군 대비 통계적으로 유의미한 차이를 보였다(p<0.02). PRO-C3는 통계적으로 유의미하지는 않았지만, 개선되는 경향을 나타냈다(p=0.06)
특히 F2-F3단계 섬유화를 동반한 MASH 환자군을 대상으로 한 하위 그룹 분석에서는 ELF Score와 PRO-C3 모두에서 통계적으로 유의미하게 개선됐다(p<0.05). F2~F3단계 섬유화를 동반한 환자는 임상 및 허가 관점에서 중요한 치료 대상으로 여겨진다.
디앤디파마텍 관계자는 “핵심 타겟 환자군인 F2-F3 동반 MASH에서 확인된 섬유화 관련 바이오마커의 지속적 개선은 48주 투여 후 시행될 간 조직생검에서 긍정적인 결과가 도출될 가능성을 시사한다”고 강조했다.
참고로 금번 24주차 분석에서는 12주차에 확인했던 MRI-PDFF 및 MRE 등 영상 기반 평가는 최초 임상 설계에 포함되지 않아 수행되지 않았다. 해당 분석은 추후 48주차에 추가로 진행될 예정이다.
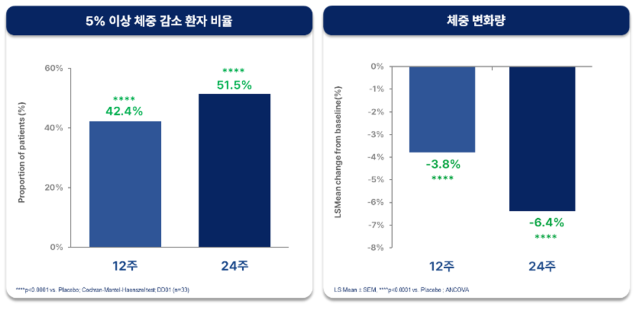
12주차에 전체 투약군 환자의 42.4%에서 체중이 5%이상 감소했다. 반면, 24주차에는 그 비율이 51.5%로 증가했다. 또한 24주 투여 후 전체 투약군 환자의 평균 체중 감소율은 6.4%로 확인됐다.
일반적으로 MASH 환자는 동반 질환이 없는 순수 비만 환자 대비 GLP-1 계열 약물의 체중 감량 효과가 약 30-40% 낮다. 이를 감안하면, DD01의 체중감소 효과는 MASH치료제는 물론 비만 치료제로서도 경쟁력 있는 결과라고 디앤디파마텍은 해석했다.
회사에 따르면 최근 MASH 치료제로 허가 받은 위고비는 MASH 임상3상에서 72주차에 10.5%의 체중감소를 보였다. 순수 비만 환자를 대상으로 한 비만 임상에서는 68주 투여 후 15~17%의 체중감소 효과를 나타냈다.
또한 DD01은 GLP‑1/글루카곤 비율을 최적화해 설계됐다. 디앤디파마텍은 MASH 환자에게 흔히 동반되는 당뇨병 관리에도 긍정적 효과를 기대한다. 이번 24주 분석에서도 12주 결과와 동일하게, DD01 투여군은 위약군 대비 당화혈색소(HbA1c)가 통계적으로 유의미하게 감소했다.
특히 당뇨병으로 진단되는 기저 당화혈색소 6.5% 이상의 환자군에서, 24주 투여 후 당화혈색소가 1.08% 감소했다. 직접비교는 어렵지만, 이는 MASH 환자를 대상으로 한 세마글루타이드 2.4mg 72주 투여 임상 결과와 유사한 수준이라는 것이 회사측의 주장이다.
최근 FDA에서 MASH 치료제 허가를 위한 비침습적 바이오마커인 VCTE 도입 검토를 시작했다. DD01 임상2상은 FDA가 검토를 시작한 초음파 기반 VCTE 보다 정확성과 신뢰성이 높은 MRE (MRI기반 간 탄성도 측정법) 분석을 포함하고 있다.
MRE는 VCTE와 달리 간 전체를 포괄적으로 측정할 수 있어 보다 정밀한 섬유화 평가가 가능한 방법으로 인정받는다.
지난 DD01 임상2상 12주 MRE 결과 전체 환자군에서 위약군 대비 통계적으로 유의미한 개선을 보였다. 이번에 추가로 수행한 12주차 하위그룹 분석에서 임상적으로 중요한 F2-F3단계 섬유화 환자군에서도 역시 동일하게 통계적으로 유의미한 차이를 확인했다.
이슬기 디앤디파마텍 대표는 “이번 24주의 긍정적인 혈액 바이오마커 결과는 MASH의 미충족 수요인 간 섬유화 개선에 직접적 상관관계가 있는 뚜렷한 지방간 감소 효과에 기인한 DD01의 치료효과가 12주차 이후에도 지속되고 있음을 보여준다”고 말했다.
그는 “DD01이 MASH와 더불어 MASH환자의 동반질환인 비만 및 당뇨를 동시에 치료할 수 있는 잠재력을 재차 보여준 결과로 해석된다”며 “이런 긍정적인 임상 결과를 토대로 앞으로도 DD01 기술이전 계약 추진에 매진해 성공적인 결과를 도출해 낼 수 있도록 최선을 다할 것”이라고 덧붙였다.