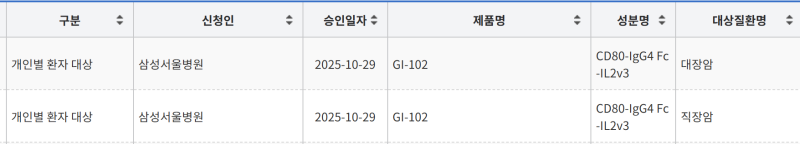
지아이이노베이션이 개발중인 면역항암제 후보물질 ‘GI-102(CD80-IgG4 Fc-IL2v3)’가 식품의약품안전처에서 대장암 및 직장암 환자에 대한 치료목적 사용승인을 받았다.
치료목적 사용승인은 생명이 위급하거나 중대한 상황에 처한 상황에서 사용할 수 있는 치료옵션이 없는 환자에 한해 연구개발 중인 약물을 사용할 수 있도록 허가하는 제도다.
30일 식품의약품안전처 의약품안전나라에 따르면 지아이이노베이션의 GI-102는 지난 29일 삼성서울병원에서 대장암과 직장암 환자에게 사용하는 것을 목적으로 2건의 치료목적 사용승인을 받았다.
GI-102는 IL-2 변이체를 가진 면역항암제 후보물질이다. 종양미세환경(TME)에서 조절 T세포(Treg)를 억제하고 자연살해(NK) 세포의 증식과 활성을 촉진하는 기전을 가진다.
올해 6월에는 난소암 환자를 대상으로 세브란스병원에서 치료목적 사용승인을 받기도 했다.
지아이이노베이션은 현재 GI-102의 SC제형 단독요법 및 PD-1 항체 ‘키트루다’와 병용요법 임상1/2상 등을 진행하고 있다.